治験管理室 一般の方へ
新しいお薬ができるまで
新しい医薬品(くすり)や医療機器を患者様に使っていただくためには、厚生労働省により、そのくすりの安全性と効果などが確認されている必要があります。そのために、この新しい「くすりの候補」を実際に患者様に使っていただき、対象となる病気に対してどのくらい効果があるのか、また安全性は大丈夫かなどを調べなければなりません。
人での有効性や安全性について調べることを「臨床試験」と言いますが、「くすりの候補」を国(厚生労働省)から「くすり」として認めてもらうために行う臨床試験のことを特に「治験」と呼んでいます。また、その治験で使用する「くすりの候補」のことを「被験薬」、被験薬と比較する目的で使用される製剤を「対照薬」といい、被験薬と対照薬の両方を「治験薬」といいます。
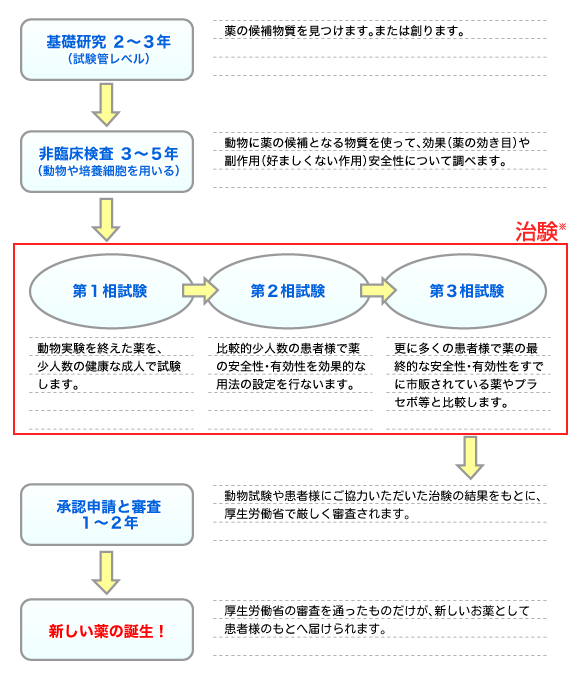
治験は下記の図のような各試験によって、効果と安全性が確かめられ、はじめてくすりとして世に出ることになります。
私達が現在使用しているくすりも、このような治験によってその効果と安全性が確認されてきたものであり、これは同時にこれまで治験に参加いただいた患者様のご協力の賜物であり、今後も病気の治療法が進歩するには不可欠なものです。
治験は、厚生労働省が定めた「医薬品の臨床試験の実施の基準」(Good Clinical Practice :GCPと呼ばれます)というルールに従って行われます。
GCPでは、以下のことが決められています。
病院は十分な設備が整っており、専門の医師をはじめとして、薬剤師、看護師、治験コーディネーターなどのスタッフが揃っていなければなりません。
- 病院は、治験の計画が治験参加者の人権や安全の保護および科学的に適切であるか審査する治験審査委員会(受託研究審査委員会)の承認と病院長の了承を得てからでなければ治験を開始できません。
- 治験審査委員会(受託研究審査委員会)は、治験に参加される方の人権と安全を保護する見地から、病院とは利害関係のない人や医学、薬学などの専門家以外の人も委員として加わります。
- 医師は、治験に参加される方に対して、治験開始前に、治験の目的、方法、有効性及び安全性などについて文書を使用して説明し、参加を希望する方から同意を文書によって取らなくてはなりません。
- 治験に参加された方のプライバシーを守らなければなりません。













